
Actualmente, gracias al código infarto, los pacientes que sufren un infarto de miocardio se tratan rápidamente para reabrir la arteria coronaria obstruida y recuperar el flujo sanguíneo al miocardio afectado. Aun así, puede aparecer una cicatriz al músculo cardíaco de estos pacientes que, si es grande, puede impedir que el corazón pueda latir correctamente, y llegar a desarrollar insuficiencia cardíaca. Para evitarlo, los investigadores del grupo ICREC liderado por el Prof. Antoni Bayés Genís, desarrollan terapias avanzadas basadas en ingeniería de tejidos y células madre para promover la reparación del corazón postinfarto.
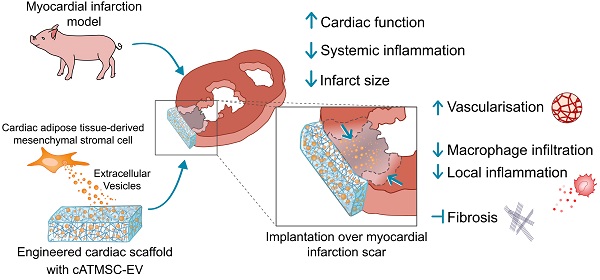
En su último estudio, publicado recientemente a Theranostics, demuestran cómo la implantación de un bioimplante cargado de vesículas extracelulares de células madre mesenquimals puede mejorar la función cardíaca en un modelo porcino de infarto agudo de miocardio. "Hemos podido ver que las vesículas extracelulares reducen la inflamación del miocardio postinfarto, favorecen la aparición de nuevos vasos sanguíneos y disminuyen el remodelado adverso que hace el corazón para adaptarse a la pérdida de capacidad muscular", comenta la primera autora del artículo, Marta Monguió-Tortajada. "Las vesículas tienen muchas de las propiedades de las células madre mesenquimales, y tienen ciertas ventajas al evitar riesgos de rechazo de trasplante y más estabilidad por no ser entidades vivas". El grupo ha contado con la colaboración del grupo REMAR-IVECAT, liderado por el Dr. Francesc E Borràs, experto en el aislamiento y caracterización de las vesículas extracelulares.
Como ya habían publicado anteriormente, la administración localizada con bioimplantes cardíacos permite una dosificación mayor en la zona diana, el miocardio infartado, consiguiendo así unos efectos locales más potentes y evitando posibles efectos secundarios. En este contexto, el grupo está evaluando asímismo si la implantación de las células madre mesenquimales (estudio PERISCOPE) es segura y tiene un efecto beneficioso en pacientes con un infarto de miocardio previo.
"La optimización de terapias como esta tienen como objetivo mejorar la vida de los pacientes, y evitar que lleguen a estadios más avanzados de insuficiencia cardíaca en los cuales el único tratamiento posible para restablecer totalmente la función cardíaca es el trasplante de corazón", explica la Dra. Carolina Gálvez-Montón, que lidera el estudio en cerdos. "Además de ser una cirugía muy invasiva, las donaciones actuales y el número incrementando de pacientes con enfermedades cardíacas hace que sea una aproximación poco sostenible".
Este trabajo ha sido financiado por la Fundación La Maratón de TV3, el Instituto de Salud Carlos III, el Ministerio de Ciencia e Innovación (MICINN y los Fondos de Desarrollo Regional de la Comisión Europea) y el Instituto Catalán de la Salud. Tanto ICREC como REMAR-IVECAT son grupos consolidados con financiación de la Agencia de Gestión de Ayudas Universitarias y de Investigación (AGAUR) de la Generalitat de Cataluña. El ICREC forma parte del área de Enfermedades Cardiovasculares del CIBER (CIBERCV) y RICORS-Terav.
Artículo de referencia
Monguió-Tortajada M, Prat-Vidal C, Martínez-Falguera D, Teis A, Soler-Botija C, Courageux Y, Munizaga-Larroudé M, Moron-Font M, Bayes-Genios A, Borràs FE, Roura S, Gálvez-Montón C. A cellular cardiac scaffolds enriched with MSC-derived extracellular vesicles límite ventricular remodelling and exert local and systemic immunomodulation in a myocardial infarction porcine model. Theranostics 2022; 12(10):4656-4670. doi:10.7150/thno.72289. Available from https://www.thno.org/v12p4656.htm